 |
Вот так
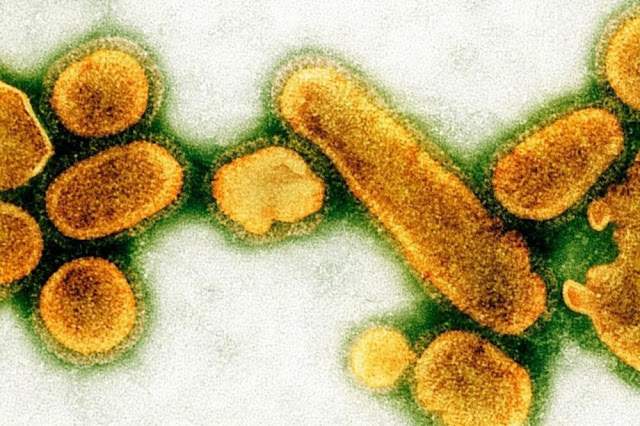
выглядел вирус испанского гриппа, в 1918 году унесшего жизни от 50 до 100 млн
человек (по разным оценкам)
|
Если бы все вирусы вдруг исчезли, мир стал бы совершенно другим - и не факт, что лучше. Что же было бы с нами без вирусов? И что значит "убить победителя"?
Глядя на пугающие картины пандемии Covid-19, разворачивающиеся, благодаря СМИ и соцсетям, перед глазами всего мира, можно подумать, что вирусы только для того и существуют, чтобы поставить человечество на колени и уморить как можно больше людей.
За прошедшее тысячелетие болезни, ими порождаемые, унесли бесчисленное количество жизней. Некоторые из вирусов убивали значительную часть населения планеты: жертвами эпидемии испанского гриппа в 1918 году стало, по разным оценкам, от 50 до 100 млн человек, еще 200 млн, как считается, умерли от оспы только в XX веке.
И нынешняя пандемия Covid-19 - лишь очередной случай из бесконечной серии нападений смертельных вирусов на человечество.
Большинство из нас сейчас, если бы нам вручили волшебную палочку и предложили ею взмахнуть, чтобы избавиться от всех вирусов на планете, с радостью согласилось бы.
Боюсь, это было бы смертельной ошибкой. Фактически, куда более смертельной, чем любой из самых свирепых вирусов.
"Если бы все вирусы вдруг разом исчезли, мир стал бы прекрасен - примерно на день-полтора. А потом мы бы все умерли, вот и всё, - говорит Тони Голдберг, эпидемиолог из Университета Висконсин-Мэдисон. - Те важнейшие вещи, за которые отвечают вирусы, значительно перевешивают зло от них".
В общем, как говорит Сусана Лопес Шаритон, вирусолог из Национального автономного университета Мексики, "без вирусов нам конец".
Большинство людей даже не догадывается о том, какую роль играют вирусы в жизни на Земле, обращая внимание только на те из них, которые нас убивают.
Почти все вирусологи изучают исключительно патогены, и только недавно несколько ученых решились исследовать вирусы, благодаря которым живы мы и наша планета.
Благодаря этой маленькой группе исследователей мы, возможно, получим более сбалансированный взгляд на мир вирусов. Оказывается, есть среди них и хорошие, причем таких - подавляющее большинство.
Но одно ученые точно знают уже сейчас: без вирусов наша планета, какой мы ее знаем, перестала бы существовать. Да и если бы мы даже задались целью истребить все вирусы на Земле, это практически невозможно.
Но представив, каким был бы мир без вирусов, мы сможем лучше понять, насколько они важны для нашего выживания, и как много нам еще предстоит узнать об этих микроскопических, простейших формах жизни, с которыми всё непросто.
За прошедшее тысячелетие болезни, ими порождаемые, унесли бесчисленное количество жизней. Некоторые из вирусов убивали значительную часть населения планеты: жертвами эпидемии испанского гриппа в 1918 году стало, по разным оценкам, от 50 до 100 млн человек, еще 200 млн, как считается, умерли от оспы только в XX веке.
И нынешняя пандемия Covid-19 - лишь очередной случай из бесконечной серии нападений смертельных вирусов на человечество.
Большинство из нас сейчас, если бы нам вручили волшебную палочку и предложили ею взмахнуть, чтобы избавиться от всех вирусов на планете, с радостью согласилось бы.
Боюсь, это было бы смертельной ошибкой. Фактически, куда более смертельной, чем любой из самых свирепых вирусов.
"Если бы все вирусы вдруг разом исчезли, мир стал бы прекрасен - примерно на день-полтора. А потом мы бы все умерли, вот и всё, - говорит Тони Голдберг, эпидемиолог из Университета Висконсин-Мэдисон. - Те важнейшие вещи, за которые отвечают вирусы, значительно перевешивают зло от них".
В общем, как говорит Сусана Лопес Шаритон, вирусолог из Национального автономного университета Мексики, "без вирусов нам конец".
 |
Некоторые вирусы сберегают
здоровье грибам и растениям
|
Большинство людей даже не догадывается о том, какую роль играют вирусы в жизни на Земле, обращая внимание только на те из них, которые нас убивают.
Почти все вирусологи изучают исключительно патогены, и только недавно несколько ученых решились исследовать вирусы, благодаря которым живы мы и наша планета.
Благодаря этой маленькой группе исследователей мы, возможно, получим более сбалансированный взгляд на мир вирусов. Оказывается, есть среди них и хорошие, причем таких - подавляющее большинство.
Но одно ученые точно знают уже сейчас: без вирусов наша планета, какой мы ее знаем, перестала бы существовать. Да и если бы мы даже задались целью истребить все вирусы на Земле, это практически невозможно.
Но представив, каким был бы мир без вирусов, мы сможем лучше понять, насколько они важны для нашего выживания, и как много нам еще предстоит узнать об этих микроскопических, простейших формах жизни, с которыми всё непросто.
 |
Без вирусов наша планета
перестала бы существовать
|
Для начала скажем, что ученым даже неизвестно, сколько всего вирусов существует. Официально классифицированы тысячи, но их - миллионы.
"Нами открыта лишь малая часть, поскольку мы особо не интересовались этим, - говорит Мэрилин Руссинк, вирусный эколог из Университета Пенн Стейт. - Таково предвзятое отношение: науку всегда прежде всего интересовали патогены".
Неизвестно ученым и то, какой именно процент всех вирусов опасен для человека. "Если смотреть на большие числа, то статистически процент опасных вирусов приближается к нулю, - говорит Кертис Саттл, вирусолог-эколог из Университета Британской Колумбии. - Почти все существующие вирусы не болезнетворны для нас".
"Нами открыта лишь малая часть, поскольку мы особо не интересовались этим, - говорит Мэрилин Руссинк, вирусный эколог из Университета Пенн Стейт. - Таково предвзятое отношение: науку всегда прежде всего интересовали патогены".
Неизвестно ученым и то, какой именно процент всех вирусов опасен для человека. "Если смотреть на большие числа, то статистически процент опасных вирусов приближается к нулю, - говорит Кертис Саттл, вирусолог-эколог из Университета Британской Колумбии. - Почти все существующие вирусы не болезнетворны для нас".